Влияние азота на свойства стали
Азот является одним из наиболее распространенных элементов: его содержание в нижних слоях атмосферы составляет 78,11% а в земной коре – 0,04%. В нормальных условиях (Т=20 °С и P=1атм) азот представляет собой 2-х атомный газ. Атомный номер – 7, атомный вес – 14,008, плотность молекулярного азота – 1,649×10-3 г/см3. Температура плавления – 209,9 °С, а температура кипения – 195,7 °С.
Исследования взаимодействия азота со сталью проводились в течении всего 20 века. Они были начаты Н.П.Чижевским и И.И.Жуковым [7]. Однако только после 40-х годов стали рассматривать возможность использования азота как легирующего элемента. Вопросам влияния азота на свойства сталей, его растворимости и поведения в металле уделялось много внимания, как в нашей стране, так и за рубежом [2…4, 8, 9]. В настоящее время в промышленности используется более 200марок сталей, легированных азотом.
Стали, легированные азотом, принято подразделять на две категории:
-стали с содержанием азота ниже равновесного;
-стали с содержанием азота выше равновесного ("сверхравновесные").
Первые получают в условиях выплавки и кристаллизации при атмосферном давлении азота. Вторые - при повышенном давлении азота, позволяющем сохранить большее его содержание в металле, чем при открытой выплавке.
В последние годы в качестве перспективных сталей с различным уровнем легирования азота для разнообразных сфер применения были отмечены [10]:
- дисперсионно-твердеющие стали, легированные ванадием, ниобием и титаном;
- высокопрочные коррозионно-стойкие, аустенитные стали;
- стали со структурой азотистого феррита и мартенсита.
Легирование азотом дисперсионно-твердеющих сталей приводит к образованию мелкодисперсных нитридов по границам зерен, препятствующих их росту, позволяет повысить предел текучести и ударную вязкость металла [8].
Легирование азотом нержавеющих сталей, позволяет уменьшить в них содержание никеля и марганца в полтора – два раза, а в некоторых случаях вообще исключить эти элементы. Нержавеющие стали, легированные азотом, превосходят по прочности, вязкости и коррозионной стойкости традиционные нержавеющие стали.
Легированные азотом безникелевые стали, применяемые в медицине для изготовления хирургического инструмента и имплантатов [11-12] обладают повышенной прочностью, износостойкостью и не вызывают негативных явлений и аллергических реакций в человеческом организме.
Нержавеющие мартенситные и ферритные стали, легированные азотом, при соответствующей термической и термопластической обработке обладают повышенной прочностью, коррозионной стойкостью и улучшенной технологической пластичностью при высоких и низких температурах.
Подробное аналитическое обобщение данных о структуре и свойствах нержавеющих сталей, легированных азотом; растворимости азота в них; термодинамике этих растворов, в том числе, в зависимости от концентрации примесей и легирующих элементов; от температур и давлений реакций, протекающих в жидком металле; параметров диффузии и других факторов, связанных с особенностями выплавки, по состоянию на 60-е годы было сделано М.В. Приданцевым, Н.П. Таловым и Ф.Л. Левиным [13].
На основе анализа многочисленных публикаций [14-17] было показано, что азот:
- образует твердые растворы внедрения в аустените и феррите;
- увеличивает количество аустенита и стабилизирует аустенит по отношению к γ → α и γ→ε превращениям при охлаждении и пластической деформации;
- изменяет предельную растворимость легирующих элементов в γ и α - твердых растворах и влияет на распределение хрома, никеля и других легирующих элементов между аустенитом и ферритом;
- изменяет кинетику образования карбидных и других избыточных фаз при термической обработке;
- снижает энергию дефектов упаковки и, в связи с этим увеличивает деформационную способность аустенита.
Введение азота в сплавы позволяет:
- уменьшить в сплавах содержание никеля, марганца и других аустенитообразующих элементов при сохранении заданной аустенитной или иной структуры и, соответственно, уровня ферромагнитности сплава;
- увеличить содержание в сплавах элементов ферритообразователей, положительно влияющих на механические и коррозионные характеристики сплавов;
- улучшить характеристики технологической пластичности в результате расширения интервала существования аустенита в высокотемпературной области;
- повысить термическую стабильность аустенита и снизить вероятность его распада при нагреве с образованием нитридов и других фаз;
- увеличить коррозионную стойкость (сопротивление питтинговой и ножевой коррозии, коррозионному растрескиванию под напряжением, интеркристаллитной коррозии);
- повысить прочность сплавов путем использования деформационного упрочнения при наклепе [1].
1.2. Растворимость азота в железе
Растворимость азота в железе подчиняется закону Сивертса (закону квадратного корня):
1/2N2 = [N]; [N] = KN (1.1)
где [N] – растворимость азота в железе при данном парциальном давлении PN2 ;
KN константа реакции, численное значение которой зависит от температуры и способов выражения концентрации.
Выполняемость закона Сивертса указывает на идеальность образующегося раствора [18].
Авторам работы [19] для определения растворимости азота в жидком железе до температуры 2650°С предлагается уравнение:
lg[N] = (-850/T) – 0,905 +0,5 lg PN2 (1.2)
Из которого следует, что при Т = 1873 °К и PN2 = 1 атм [N] = 0,044%.
Анализ результатов многих исследований, выполненных различными авторами [18-25] методом отбора проб, показал хорошую согласованность данных, уровень отклонения которых от расчетной величины составляет 0,002%.
На рис.1.1 представлена температурная зависимость растворимости азота в жидком железе. Диаграмма состояния системы железо-азот приведена на рис. 1.2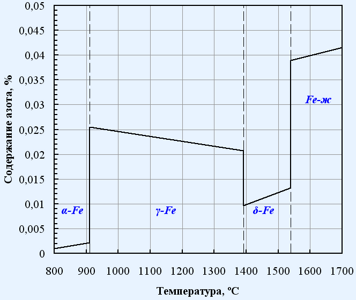 . .
Рис. 1. 1. Температурная зависимость растворимости азота в жидком железе

Рис.1.2. Диаграмма состояния Fe-N [26]
Концентрация азота, находящегося в равновесии с газообразным азотом растет с увеличением температуры. В точке перехода α→γ (906 °С) скачкообразно изменяется, при дальнейшем росте температуры до перехода γ→ δ (1402 °С) она уменьшается.
Азот может образовывать с железом два соединения Fe4N (9,9% N) и Fe2N (11,5% N). Fe2N начинает разлагается при температуре ~550 °С. При дальнейшем повышении температуры начинает диссоциировать и Fe4N.
Энтальпия растворения азота в жидком железе ΔHN представляет собой разность двух противоположных по знаку величин: энтальпии диссоциации молекулярного азота на атомы (ΔHдис) и энтальпии растворения атомарного азота в жидком железе (ΔHP). Первый процесс является эндотермическим, а второй – экзотермическим. Так как ΔHдис > ΔHP, то процесс, описанный уравнением (1), протекает с поглощением тепла. Если данные по растворимости азота показывают хорошую согласованность у различных исследователей, то данные по энтальпии имеют значительный разброс.
Результаты статистической обработки большого массива экспериментальных данных позволили авторам работы [27] описать растворимость азота в жидком железе двумя уравнениями:
при Т < 1973K: lg [N] = -560/T – 1,06 (1.3)
при Т > 1973K: lg [N] = -1100/T – 0,79 (1.4)
Таким образом, энтальпия растворения азота в жидком железе до 1973 °K – 10700 Дж/моль, а выше 1973 °K – 21000 Дж/моль.
А.М. Самарин, первым обративший на это внимание, связывал изменение ΔH при изменении температуры со структурными превращениями. Известно, что при растворении кислорода оксидная фаза проявляется при очень низком парциальном давлении кислорода в газовой фазе ( PO2= 10-8 атм). В отличие от этого, при растворении азота даже при PN2 > 1атм самостоятельная нитридная фаза не образуется. Образование нитридов типа Fe2N и Fe4N наблюдали лишь в твердом металле в температурном интервале существования аустенита.
Влияние парциального давления над расплавом железа на его растворимость в зависимости от времени выдержки при T = 1560 °C представлено на рис. 1.3.
Данные по кинетике азотирования свидетельствуют о том, что для выхода на стационарную концентрацию в чистом железе требуется около 40 мин., причем время практически не зависит от давления азота над расплавом.

Рис. 1.3. Изменение растворимости азота в железе в зависимости от его давления и времени выдержки при температуре 1560 °С [28].
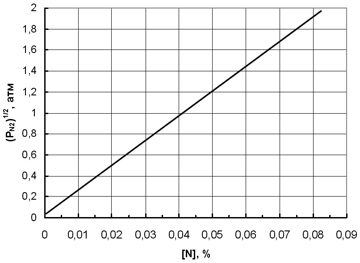
Рис.1.4. Зависимость растворимости азота в жидком железе при температуре 1560 °С от парциального давления азота над расплавом
Присутствие примесей влияет на скорость растворения азота в металле. Так, при увеличении концентрации кислорода в металле от 0,067 до 0,144% время достижения равновесной концентрации увеличивается с 1,5 до 3,0 часов. Отмечено и аналогичное влияние серы: при ее концентрациях 0,49 и 0,87% и давлении азота 0,1МПа время достижения равновесной концентрации возрастает до 3,0 и 6,0 часов соответственно.
В работе [14] представлены данные, характеризующие изменение растворимости азота в жидком железе при температуре 1560 °С в зависимости от давления (до 4 атм.).
Список использованой литературы
1. Костина М.В. Развитие принципов легирования Сr- N сталей и создание коррозионно-стойких сталей нового поколения со структурой азотистого мартенсита и аустенита для высоконагруженных изделий современной техники. – Дис. … д-р тех. наук. – М.: ИМЕТ РАН, 2003.- 231 с.
2. Самарин А.М. Замена никеля азотом в жароупорной стали. // Известия АН СССР. ОТН - 1944.- № 1-2.
3. Просвирин В.И., Агапова Н.П. Влияние азота на свойства стали с высоким содержанием хрома. Сб. трудов /ЦНИИТМАШ "Азот в стали" -М.: Машгиз, № 1950.-№29.
4. Рашев Ц.В. Высокоазотистые стали. Металлургия под давлением.- София:- Издательство Болгарской академии наук "Проф. Марин Дринов",1995. -218с.
5. Poschitz I.N., Kolesov V.A. Use of High-Nitrogen non magnetic steel for production of steel-aluminum conductor. 5-th Int. Conf. High Nitrogen Steels. Espoo – Finland. may 27-28. 1998 (Далее HNS-98). Book of Abstracts. -Р. 19.
6. Банных О.А. Блинов В.М. Костина М.В., Лякишев Н.П., Ригина Л.Г., Горынин И.В., Рыбин В.В., Малышевский В.А., Калинин Г.Ю., Ямпольский В.Д., Буцкий Е.В., Римкевич В.С., Сидорина Т.Н. «Высокопрочная немагнитная коррозионно-стойкая свариваемая сталь». Патент РФ № 2205889, 2002.
7. Банных О.А. Блинов В.М. Костина М.В., Малышевский В.А., Рашев Ц.В., Ригина Л.Г., Дымов А.В., Устиновщиков Ю.И. «Высокопрочная коррозионно и износостойкая немагнитная сталь». Патент РФ № 2158319, 2000.
8. Чижевский Н.П. Железо и азот. Томск. -1914.
9. Банных О.А., Блинов В.М. Дисперсионно-твердеющие немагнитные ванадий содержащие стали. -М.: Наука. 1980. -192с.
10. Berns H. Alloy development and processing. Int. Conf. High Nitrogen Steels. HNS-2004. Book of abstracts. -P. 271-281.
11. Гаврилюк В.Г., Ефименко С.П. Влияние азота на структуру и свойства и -железа и перспективные направления разработки высокоазотистых сталей . Труды Iой Всесоюзной конференции "Высокоазотистые стали". Киев 18-20 апреля 1990. -С. 5-26.
12. Ефименко С.П., Пановко В.М., Лещинская Е.М., Сокол И.Я., Ригина Л.Г., Мишина Е.Г., Гаврилюк В.Г., Марков Б.П. «Коррозионно-стойкая немагнитная износостойкая сталь ». Патент РФ № 2116374, 1996.
13. Приданцев М.В., Талов Н.П., Левин Ф.М. Высокопрочные аустенитные стали. –М.: Металлургия, 1969.- 247с.
14. Рашев Ц. Производство легированной стали. -М.: Металлургия, 1981. - 246 с.
15. Костина М.В., Банных О.А., Блинов В.М. Особенности сталей легированных азотом. // Металловедение и термообработка.- 2000. -№12.- С. 3-6.
16. Nakamura N., Tsuchiyma T., Takaki S. Effect of structural factors of the mecanical properties of the high nitrogen austenitic steels. HNS-98. Book of Abstracts. -P. 209-214.
17. Блинов В.М., Елистратов А.В., Колесников А.Г. и др. Влияние термической обработки на структурные превращения и свойства высокоазотистых сталей. //Металловедение и термообработка.- 2000.- № 6. -С. 19-24.
18. Григорян В.А., Белянчиков Л.Н., Стомахин А.Я. Теоретические основы электросталеплавильных процессов. -М.: Металлургия, -1987.-136с.
19. Свяжин А.Г., Чурсин Г.М., Вишкарев А.Ф., Явойский В.И. //Металлы.- 1974.- № 5.- С.23-35.
20. Аверин В.В., Ревякин А.В., Федорченко В.И., Козина Л.Н. Азот в металлах. -М.: Металлургия,- 1976.- 221с.
21. Martin E. // Arhiv Eisenhuttenw. -1929/30.- Bd.3. -S.314.
22. Sieverts A. //Z. Phys. Chem. -1938.- Bd. A 155.- S. 229.
23. Sieverts A., Zapf G. // Z. Phys. Chem.- 1938. Bd. 178. -S. 314.
24. Pelke R.D.,Elliot I.F. The Solubiliny of Nitrogen in Liquid Iron Alloys.// Trаnsaction of the Metallurgical Society of AIMЕ. -1963.- V. 227. -№5. -P.849-855.
25. Морозов А.И. Водород и азот в стали.- М.: Металлургиздат, 1968. -280с.
26. Наnsen M., Anderko K. Constitution of binary alloys. -1959.- P. 539-541.
27. Юрин В.В., Котельников Г.И., Стомахин А.Я., Григорян В.А. Температурная зависимость растворимости азота в жидком железе. // Известия вузов. Черная металлургия. -1986.- № 11. -С.40-45.
28. Shenck H., Frohberg M.,Heineman H. Untersuchungen zur stickstoff aufnahme in flussigen Druckbericht lis zu vier Atmosfiran. // Eisenlegirungen in Archiv fur Eisenhuttenw. 1962.-B.33. №9. S. 503-602.
|